El pez payaso (subfamilia Amphiprioninae) es una especie marina emblemática, reconocida mundialmente por su relación simbiótica con las anémonas. Destaca por su naturaleza como hermafrodita protándrico —capaz de realizar una transición de sexo—, su excepcional inmunidad ante toxinas urticantes y su alta valoración en el mercado de especies ornamentales. Ante el drástico descenso de sus poblaciones silvestres, la acuicultura ha emergido como la solución sostenible para satisfacer la demanda global.
Tanto si es un entusiasta de los arrecifes que desea recrear un ecosistema oceánico en casa, como si es un acuarista profesional en busca de nuevos desafíos, esta guía técnica es el recurso definitivo para garantizar un entorno próspero. A lo largo de este contenido, analizaremos desde sus rasgos evolutivos hasta los parámetros técnicos críticos para el éxito en la acuicultura y el acuarismo avanzado.
Desde la comprensión de sus necesidades biológicas hasta el dominio del mantenimiento técnico, le guiaremos a través del complejo cuidado de estas fascinantes criaturas. Descubra las claves para configurar el acuario ideal, proporcionar una nutrición equilibrada y diseñar un hábitat armónico que replique con exactitud su entorno natural.
- 1 Puntos Clave: Lo que debe saber sobre el Pez Payaso
- 2 Clasificación y Diversidad de las Especies
- 3 Distribución Geográfica y Entorno Natural
- 4 La Simbiosis: El Arte de la Coevolución
- 5 Nutrición y Estrategias de Alimentación
- 6 Reproducción y Dinámicas de Género
- 7 Mantenimiento y Parámetros de Calidad del Agua
- 8 Compatibilidad y Dinámicas de Convivencia
- 9 Patologías Comunes y Gestión Sanitaria
- 10 Conclusión
-
11
Preguntas Frecuentes (FAQ) sobre el Pez Payaso
- 11.1 ¿Realmente todos los peces payaso nacen machos?
- 11.2 ¿Cuál es la temperatura ideal para que no tengan malformaciones?
- 11.3 ¿Es obligatorio usar Artemia para alimentar a las larvas?
- 11.4 ¿Cómo puedo intensificar el color de mis peces?
- 11.5 ¿Por qué mi pez payaso es agresivo con otros peces?
- 11.6 ¿Qué importancia tiene la oscuridad en la eclosión de los huevos?
- 12 Referencias bibliográficas
- 13 Entradas relacionadas:
Puntos Clave: Lo que debe saber sobre el Pez Payaso
- Biología de Transición: Son hermafroditas protándricos. El cambio de sexo de macho a hembra es irreversible y está regulado por el modelo ARCH (Arquetipo, Impulso, Contexto y Fase), una decisión biológica compleja y no meramente lineal.
- Simbiosis y Coevolución: La relación con las anémonas no es al azar. Los peces seleccionan linajes específicos de anémonas con los que han coevolucionado; por ejemplo, la anémona «burbuja» (E. quadricolor) actúa como un complejo de especies especializado para diferentes tipos de peces payaso.
- Optimización del Crecimiento: La temperatura ideal de cultivo oscila entre 28 °C y 30 °C. Superar los 31 °C acelera el crecimiento en un 16%, pero alcanzar los 34 °C dispara el riesgo de malformaciones esqueléticas (como la lordosis) hasta un 13.3%.
- Revolución en la Larvicultura: Es posible eliminar la dependencia de la Artemia viva. Realizar un destete temprano hacia microdietas inertes a los 5 días de la eclosión puede aumentar la ganancia neta en aproximadamente $1.60 USD por pez.
- Potenciación del Color: La suplementación con astaxantina (mínimo 0.5%) o extractos naturales de fruto de Gac y pimiento morrón es esencial para la industria ornamental, logrando incrementos de pigmentación roja superiores al 75%.
- Eficiencia Hídrica y Económica: Los juveniles pueden desarrollarse con un 95% de supervivencia en salinidades bajas de 15‰. Esta estrategia de agua salobre permite un ahorro de hasta el 57% en costos de sales comerciales.
- Bienestar y Entorno: El color del tanque influye en la salud. El uso de tanques de colores oscuros en lugar de blancos reduce drásticamente los niveles de cortisol (estrés) en las larvas, mejorando su respuesta ante patógenos.
- Gestión de la Eclosión: Para una eclosión exitosa y sincronizada, es crítico garantizar oscuridad absoluta y agitación mecánica del agua durante la noche del octavo día post-desove.
Clasificación y Diversidad de las Especies
Actualmente, se reconocen 30 especies de peces payaso (también denominados peces anémona), distribuidas principalmente en los géneros Amphiprion y Premnas. Entre las variedades más emblemáticas destacan el Amphiprion ocellaris (falso payaso), el Amphiprion percula (percula real) y el Premnas biaculeatus (payaso marrón), los cuales se distinguen morfológicamente por sus patrones de coloración y el conteo de espinas dorsales.
Aunque el Amphiprion ocellaris es frecuentemente confundido con el A. percula, estudios recientes han redefinido nuestra comprensión de su linaje. Según Gaboriau et al. (2025), tras la secuenciación del genoma completo de las 28 especies principales, se estableció el árbol filogenético más robusto hasta la fecha. Este estudio revela que el Amphiprion biaculeatus representa un linaje basal para el resto del grupo. Asimismo, los hallazgos sugieren que el ancestro común de estos peces era un generalista ecológico, y que la especialización hacia anfitriones específicos (anémonas) fue un proceso evolutivo que ocurrió de forma recurrente en su historia.
En el ámbito cultural, el Amphiprion percula alcanzó la fama mundial gracias a la cinematografía; no obstante, en la industria ornamental, el Amphiprion ocellaris es la especie predilecta debido a su notable resiliencia y facilidad de reproducción en cautiverio.
Perfil Taxonómico
A continuación, se detalla la clasificación científica de la subfamilia Amphiprioninae:
- Filo: Chordata
- Clase: Actinopterygii
- Clado: Percomorpha
- Familia: Pomacentridae
- Géneros: Amphiprion y Premnas
- Especies representativas: A. percula, A. ocellaris, A. clarkii, P. biaculeatus.
- Nomenclatura común: Peces payaso, peces anémona, Clownfish.
Anatomía y Adaptaciones Evolutivas
El linaje evolutivo de los peces payaso divergió hace aproximadamente 35 millones de años, desarrollando adaptaciones biológicas extraordinarias que garantizan su supervivencia en los arrecifes:
- Visión Ultravioleta (UV): Poseen la capacidad de percibir el espectro ultravioleta, una herramienta evolutiva clave para identificar anémonas anfitrionas y reconocer a otros miembros de su grupo social.
- Comunicación Acústica: Son capaces de producir sonidos mediante el choque de sus mandíbulas. Estas vibraciones son amplificadas por la vejiga natatoria y se utilizan principalmente como advertencia para la defensa del territorio.
- Dimorfismo Sexual y Tamaño: Existe un marcado dimorfismo sexual en el que las hembras presentan un tamaño superior al de los machos. Dependiendo de la especie, la longitud puede oscilar entre los 7 cm y los 17 cm.
Visualmente, estas especies son fascinantes. Presentan coloraciones que van desde el amarillo y el naranja vibrante hasta tonos rojizos y negruzcos, generalmente acentuados por parches o barras blancas. Comprender estos rasgos morfológicos y los comportamientos específicos de cada especie le permitirá tomar una decisión informada para garantizar un ecosistema equilibrado en su acuario.
Mantente siempre informado
Únete a nuestras comunidades para recibir al instante las noticias, informes y análisis más importantes del sector acuícola.
Principales Especies y Variedades de Diseño
En el mercado acuariofilo, la selección de la especie adecuada es fundamental para el éxito del tanque:
Variedades de Diseño (Designer Clownfish)
Gracias a los avances en la acuicultura selectiva, hoy disponemos de patrones morfológicos únicos. Ejemplares como el Orange Storm, Black Frostbite o el Snowflake son piezas de colección altamente valoradas en la industria ornamental contemporánea.
«Falso payaso» Amphiprion ocellaris
Es el ejemplar más popular en la acuicultura. Se caracteriza por poseer 11 espinas dorsales y una coloración naranja brillante sumamente atractiva.

Amphiprion percula
Frecuentemente confundido con el ocellaris, se distingue por tener bordes negros más gruesos en sus franjas blancas y 10 espinas dorsales.

Amphiprion clarkii
Conocido como el pez payaso de cola amarilla (A. clarkii). Las hembras de esta especie pueden alcanzar los 15 cm, mientras que los machos solo 10 cm.

Premnas biaculeatus (Pez Payaso Marrón)
Destaca por su imponente tamaño (hasta 17 cm) y un temperamento notablemente más territorial y agresivo.

Distribución Geográfica y Entorno Natural
Los peces payaso son originarios de las aguas tropicales de los océanos Pacífico e Índico. Su distribución abarca ecosistemas críticos como el Mar Rojo, la Gran Barrera de Coral de Australia, el Sudeste Asiático, las costas de Japón y la biodiversa región de Indo-Malasia. En estos entornos, su presencia está intrínsecamente ligada a la salud de los arrecifes coralinos y la disponibilidad de anémonas hospederas.
En su estado silvestre, estas especies exhiben una de las estructuras sociales más fascinantes del mundo marino. Los grupos se organizan mediante una jerarquía estricta basada en el tamaño y la dominancia:
- Matriarcado Dominante: Las comunidades están lideradas por una hembra, que es el individuo de mayor tamaño y autoridad.
- Vínculos de Pareja: Forman parejas reproductoras exclusivas. Tras la hembra, el macho más grande ocupa el segundo rango en la escala social.
- Roles de Supervivencia: El macho asume la responsabilidad crítica de defender el territorio frente a intrusos y asegurar el sustento para la hembra y la progenie, garantizando así la viabilidad de la puesta.
Comprender estas dinámicas naturales es un requisito indispensable para cualquier acuarista, ya que permite replicar un entorno armonioso que respete los instintos biológicos de estas cautivadoras criaturas en el acuario doméstico.
La Simbiosis: El Arte de la Coevolución
Mutualismo y Protección Química
La relación entre el pez payaso y la anémona representa uno de los ejemplos más perfectos de mutualismo en el reino marino. Mientras que el contacto con los nematocistos (células urticantes) de la anémona resultaría letal para otras especies, el pez payaso ha desarrollado una mucosa protectora especializada que inhibe la respuesta de disparo de los tentáculos, volviéndose virtualmente «invisible» para su anfitrión.
Este vínculo ofrece beneficios bidireccionales: la anémona proporciona un refugio inexpugnable contra depredadores, mientras que el pez defiende activamente a su anfitriona de parásitos y peces mariposa, además de proporcionarle nutrientes vitales a través de sus desechos nitrogenados.
Clasificación por Especialización y Fenotipo
La ciencia ha profundizado en cómo esta asociación moldea la apariencia de los peces. Según Maison y Graham (2016), especies como el A. percula se vinculan principalmente con Heteractis crispa, H. magnifica y Stichodactyla gigantea. Por su parte, la investigación de Gaboriau et al. (2025) revela que los peces payaso han evolucionado en cuatro categorías morfológicas basadas en su hábitat reproductivo y su anémona específica:
- Generalistas: Presentan cuerpos oscuros con dos o tres bandas blancas; su morfología es versátil y similar a los especialistas en Entacmaea.
- Especialistas en Radianthus magnifica: Poseen cuerpos más alargados, pedúnculos caudales robustos y una coloración naranja clara con rayas reducidas.
- Especialistas en Entacmaea quadricolor: Caracterizados por un tono naranja rojizo, hocico corto, cuerpo más profundo y un menor grosor en sus marcas blancas.
- Especialistas en Stichodactyla: Un grupo evolutivo altamente diferenciado y adaptado exclusivamente a este género de anémonas.
Reclutamiento y Selección Genética
Nuevas evidencias aportadas por Chiodo et al. (2026) sugieren que la anémona «burbuja» (Entacmaea quadricolor) no es una sola especie, sino un complejo de linajes diversos cuya evolución ha sido moldeada por sus simbiontes. Este estudio es crucial, ya que demuestra que el asentamiento de los peces payaso en el arrecife no es aleatorio; los peces «reclutan» o seleccionan específicamente linajes de anémonas con los que han coevolucionado durante milenios.

Nutrición y Estrategias de Alimentación
Garantizar una dieta equilibrada es el pilar fundamental para la vitalidad y el crecimiento óptimo del pez payaso. En su hábitat natural, esta especie mantiene una dieta omnívora, basada principalmente en zooplancton, pequeños crustáceos y materia vegetal (algas). En cautiverio, el éxito radica en replicar esta diversidad nutricional mediante un enfoque multifacético.
Directrices para el Acuario Doméstico
Para mantener la salud de sus ejemplares, se recomienda una dieta variada que combine:
- Alimentos secos: Gránulos y escamas de alta calidad nutricional.
- Alimentos frescos/congelados: Artemia, mysis y mezclas de mariscos.
- Frecuencia: Es preferible suministrar pequeñas raciones varias veces al día. Esta práctica imita su comportamiento de forrajeo natural y previene la degradación de la calidad del agua por exceso de residuos.
Avances en Acuicultura y Dietas Especializadas
La investigación reciente ha introducido componentes críticos para optimizar la cría profesional:
- Fuentes Alternativas de Proteína: Según Vargas et al. (2019), la inclusión de harina de insectos (Hermetia illucens) es una alternativa sostenible que no compromete el crecimiento ni la respuesta al estrés de los juveniles.
- Nutrición para Reproductores: Para el Amphiprion ocellaris, Roux et al. (2021) sugieren dietas ricas en ácidos grasos poliinsaturados, compuestas por una mezcla de calamar, mejillones, camarón y alga nori.
- Optimización del Color: La pigmentación es clave en el mercado ornamental. Mientras Díaz-Jiménez et al. (2021) recomiendan un mínimo de 0.5% de astaxantina, el estudio de Tran et al. (2024) propone el uso de carotenoides naturales (Gac y pimiento morrón), logrando incrementos de hasta un 89% en la intensidad del color rojo.
- Salud Probiótica: La suplementación con Lactobacillus plantarum (10⁶ a 10⁸ UFC/g) mejora significativamente el rendimiento zootécnico y fortalece el sistema inmunológico contra patógenos como Vibrio fluvialis (Paixão et al., 2020).
Larvicultura: El Desafío del Desarrollo
El éxito en la cría de larvas ha dependido históricamente del uso de alimento vivo especializado, como los rotíferos (Brachionus plicatilis) y microalgas como Nannochloropsis oculata. No obstante, investigaciones recientes están transformando los protocolos tradicionales para maximizar la supervivencia y reducir costos operativos.
Avances en Protocolos de Alimentación y Destete
Tradicionalmente, autores como Nass et al. (2016) sugerían la introducción de nauplios de Artemia apenas dos días después de la eclosión para especies como Amphiprion clarkii. Sin embargo, el estudio de Murray et al. (2025) sobre Amphiprion ocellaris marca un hito al demostrar que es posible reducir drásticamente la dependencia de organismos vivos costosos.
A continuación, se detallan los hallazgos más disruptivos para la industria:
- Transición Temprana y Resistencia: Las larvas pueden realizar la transición de rotíferos a Artemia a los 5 días posteriores a la eclosión (DPH) sin comprometer su longitud total ni elevar sus niveles de cortisol corporal (indicador de estrés).
- Eliminación de la Fase de Artemia: El hallazgo más significativo revela que las larvas pueden prescindir totalmente de la Artemia si se introduce una microdieta inerte a tiempo. Iniciar el suministro de microdietas comerciales a los 5 DPH garantiza una tasa de supervivencia superior (64%), superando los resultados de destetes tardíos (8 u 11 DPH). Cabe destacar que el alimento inerte no debe suministrarse desde el primer día, pues la supervivencia inicial depende estrictamente del estímulo del alimento vivo.
- Calidad Estética y Valor Comercial: La elección de la microdieta influye directamente en la rentabilidad. El uso de alimentos suplementados con astaxantina (como TDO Chroma Boost™) produce ejemplares con una saturación de color y brillo superiores, factores determinantes en el valor de mercado de los peces ornamentales.
Impacto Económico en la Acuicultura
La implementación de estos nuevos protocolos no solo optimiza la biología del pez, sino también las finanzas del productor. Al eliminar el uso de Artemia y transicionar directamente de rotíferos a microdieta a los 5 DPH, se estima un ahorro operativo que se traduce en un incremento de la ganancia neta de aproximadamente $1.60 USD por cada ejemplar producido.
Alimentación de Juveniles y Optimización de la Pigmentación
Una vez superada la etapa larval, la nutrición de los juveniles se enfoca en consolidar el crecimiento y, fundamentalmente, en el desarrollo de una coloración competitiva para el mercado ornamental.
El Impacto de la Astaxantina Natural
Según la investigación reciente de Hoffmann et al. (2025), la suplementación estratégica con astaxantina es el método más eficaz para potenciar la vitalidad cromática de los juveniles de Amphiprion ocellaris. Los hallazgos clave de este estudio incluyen:
- Eficiencia Biológica: El uso de fuentes naturales de la microalga permite obtener resultados estéticos superiores en un tiempo de exposición menor comparado con dietas estándar, lo que optimiza los ciclos de producción en cautiverio.
- Fuente de Alta Disponibilidad: Se recomienda una dosis de 18 mg por kilogramo de alimento, derivada específicamente de la microalga Haematococcus pluvialis, reconocida por su alta concentración de pigmentos naturales.
- Resultados en Tiempo Récord: Tras un periodo de alimentación de apenas 60 días, se demostró una mejora drástica en la intensidad del tono rojo. Los científicos observaron una pigmentación notablemente más vibrante en zonas críticas como la región ventral y las aletas pectorales.
Reproducción y Dinámicas de Género
El sistema reproductivo de los peces payaso es uno de los mecanismos más singulares del mundo marino. Son hermafroditas protándricos: todos los individuos nacen machos y se organizan en jerarquías sociales estrictas donde solo el ejemplar más grande y dominante realiza la transición biológica a hembra.
El Modelo ARCH y el Cambio de Sexo
Contrario a la creencia popular de que el cambio de sexo es una respuesta lineal y simple ante la ausencia de una hembra, el estudio de Rahman (2026) revela una complejidad mayor. Este proceso es una «decisión biológica» gobernada por el modelo ARCH (Arquetipo, Impulso, Contexto y Fase). Según este modelo multiplicativo, el cambio solo se activa cuando se superan ciertos umbrales hormonales y sociales específicos, garantizando que la transición sea exitosa y permanente.
En una anémona o acuario típico, la estructura se divide en:
- Hembra Alfa: El individuo dominante y de mayor tamaño, responsable de la puesta de huevos.
- Macho Reproductor: El segundo en el rango y el único encargado de la fecundación.
- Juveniles No Reproductores: Individuos con desarrollo frenado para evitar conflictos jerárquicos.
Protocolos de Cría y Manejo en Cautiverio
La cría exitosa en acuarios es posible si se imitan las condiciones naturales. Investigaciones de Lai et al. (2026) sugieren parámetros exactos para la hibridación y cría de Amphiprion ocellaris:
- Dimensiones Óptimas: Se recomienda un ratio de tamaño de 2.5 ± 1 cm para machos y 5 ± 1 cm para hembras.
- Técnica de Introducción: Para reducir la agresividad, se debe introducir primero al macho pequeño y, tras 12 horas, a la hembra. Esto permite que el macho establezca su territorio, facilitando el emparejamiento.
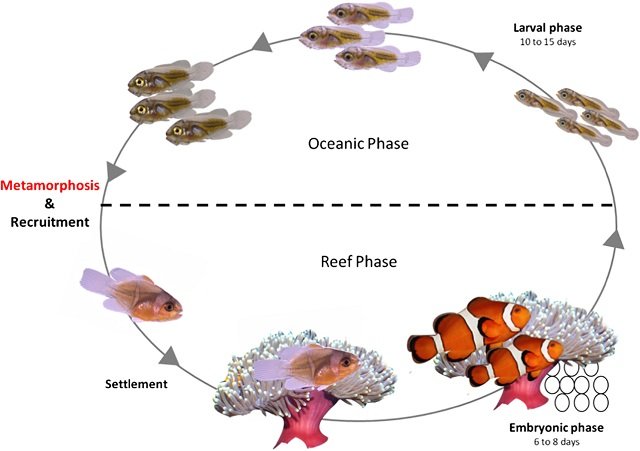
El Ciclo de Vida: Del Huevo a la Eclosión
La hembra del pez payaso, dependiendo de la especie, deposita entre 600 y 1,500 huevos en una superficie plana cerca de la protección de la anémona. El macho asume el rol de cuidador, encargándose de la oxigenación y la eliminación de huevos no viables.
Un factor crítico a considerar es la contaminación lumínica. Según Fobert et al. (2020), la exposición a luz artificial durante la noche altera el ciclo lunar reproductivo, reduciendo drásticamente la tasa de eclosión. Por ello, el control del fotoperiodo es esencial para cualquier proyecto de acuicultura.
Preferencias de Desove y Entorno
En ausencia de anémonas naturales, la elección del sustrato es determinante. Según Lai et al. (2026), especies como Amphiprion ocellaris muestran una preferencia selectiva por superficies de textura rugosa, como baldosas o macetas de cerámica huecas, rechazando materiales lisos o sintéticos como el PVC. Este comportamiento sugiere que los reproductores priorizan entornos que ofrezcan mayor privacidad y seguridad para la puesta.
En términos de volumen, estudios en Amphiprion clarkii (Sarvi y Pourmozaffar, 2024) reportan puestas de entre 300 y 400 huevos, mientras que en A. ocellaris el ciclo de vida y los protocolos de crianza larval han sido documentados extensamente por Roux et al. (2019, 2021).

El Factor Temperatura en el Desarrollo Embrionario
La temperatura del agua actúa como el principal regulador del metabolismo embrionario. Rodríguez-Ibarra et al. (2024) determinaron que, aunque la supervivencia larvaria es óptima en un amplio rango, existen puntos críticos:
- Eficiencia Térmica: A 30 °C se registran los mayores índices de éxito, con un 98.2% de eclosión y un 96% de supervivencia.
- Velocidad de Desarrollo: El incremento térmico acelera el proceso; a 34 °C, la eclosión ocurre a las 144 horas post-fertilización, comparado con las 168 horas requeridas a temperaturas inferiores (26-30 °C).
Protocolo de Eclosión Sincronizada
Para maximizar los resultados comerciales, Yamanaka et al. (2025) recomiendan un protocolo específico durante la noche del octavo día tras el desove:
- Agitación Mecánica: El movimiento del agua acelera la digestión de la envoltura del huevo, permitiendo una eclosión rápida y, sobre todo, sincronizada.
- Oscuridad Absoluta: Es el detonante biológico para la secreción de las enzimas de eclosión.
Larvicultura del pez payaso
La crianza larval representa el desafío técnico más exigente en la acuicultura ornamental. Según Tartila et al. (2023), este proceso requiere una gestión rigurosa que abarca desde la preparación del medio y la siembra de huevos hasta el manejo de sistemas de recirculación (RAS) y la cosecha final.
Dinámica Térmica y Crecimiento Acelerado
La temperatura es el motor metabólico del desarrollo larval. Investigaciones recientes presentan matices clave para maximizar la eficiencia:
- Desarrollo y Morfología: Moore et al. (2023) demostraron que las larvas de A. ocellaris criadas a 31 °C se desarrollan significativamente más rápido, alcanzando etapas críticas en solo 8 días y mostrando un incremento del 16% en longitud y diámetro ocular respecto al estándar.
- Límites Biológicos: Aunque Rodríguez-Ibarra et al. (2024) señalan que el crecimiento máximo ocurre a 34 °C, advierten que el rango ideal para evitar malformaciones se sitúa entre 28 y 30 °C.
- Optimización por Especie: Para A. clarkii, Medeiros et al. (2026) recomiendan una combinación de 30 °C y una salinidad reducida de 20‰. Este hallazgo es crucial para instalaciones tierra adentro, ya que permite reducir costos en sal sintética sin comprometer el crecimiento.
El Rol del Cuidado Parental y la Fisiología Digestiva
Antes de la eclosión, la intervención del macho es determinante. Arossa et al. (2025) reportan que el cuidado parental (abanicado y frotado) incrementa los niveles de oxígeno en la masa de huevos en un 51%, protegiendo a los embriones de la hipoxia local.
Tras la eclosión, las larvas muestran una madurez sorprendente. Sarvi y Pourmozaffar (2024) destacan que poseen un sistema digestivo desarrollado y una apertura bucal de 250 µm, permitiéndoles consumir rotíferos estándar de inmediato. La formación temprana de glándulas gástricas (entre los 11 y 15 días) facilita una transición eficiente hacia dietas artificiales.
Etología y Bienestar: El Impacto del Color
El entorno físico influye directamente en la salud hormonal. Un estudio de dos Santos et al. (2023) desaconseja el uso de tanques blancos para la cría de Amphiprion frenatus. Se descubrió que las larvas adaptadas a fondos claros muestran niveles de cortisol (estrés) significativamente más altos ante estímulos agudos. El uso de tanques de colores oscuros o neutros promueve un estado de bienestar superior y una mejor respuesta inmunológica.
Crianza de Juveniles: Sociabilidad y Manejo del Estrés
Una vez que las larvas completan su metamorfosis, el manejo de los ejemplares juveniles requiere una comprensión profunda de sus instintos sociales. La investigación de Wang et al. (2025) sobre el Amphiprion ocellaris aporta pautas críticas para la organización de las poblaciones en cautiverio.
Estrategias de Agrupamiento y Supervivencia
El estudio revela que los juveniles, independientemente de su talla (desde los 2.0 cm hasta los 4.0 cm), poseen un alto grado de sociabilidad, mostrando una preferencia constante por permanecer cerca de sus congéneres. No obstante, existen diferencias conductuales según el tamaño:
- Juveniles Pequeños (2.0–2.5 cm): Presentan una tendencia mucho más acusada al agrupamiento estrecho, una estrategia evolutiva vinculada a la protección colectiva frente a potenciales depredadores.
- Juveniles Grandes (3.5–4.0 cm): Aunque son sociables, dependen más de la estabilidad de su entorno y de grupos ya conocidos para mantener niveles bajos de estrés.
Recomendaciones para la clasificación
Basándose en estos hallazgos, se sugiere que los procesos de clasificación o separación por tallas de los peces payasos juveniles se realicen de manera temprana. Implementar estas medidas antes de que los ejemplares alcancen tamaños superiores minimiza los conflictos territoriales y el estrés social. Realizar la transición en etapas iniciales garantiza una mayor tasa de supervivencia, ya que evita desestabilizar los vínculos sociales complejos que los peces más grandes establecen con su entorno.
Mantenimiento y Parámetros de Calidad del Agua
El éxito a largo plazo en la crianza de peces payaso depende de la estabilidad del entorno. Mantener parámetros fisicoquímicos óptimos no solo garantiza la supervivencia, sino que maximiza el crecimiento y la rentabilidad de la instalación.
Densidad de Cultivo y Nutrición
Para ejemplares de A. percula, Chambel et al. (2015) establecen que la densidad óptima para obtener un factor de condición superior es de 2 peces por litro. Asimismo, se determinó que una dieta con un 41% de proteína cruda es el estándar de oro para promover un crecimiento vigoroso durante la etapa juvenil.
Gestión de la Temperatura y Estrés Térmico
Aunque el rango de tolerancia para A. ocellaris abarca desde los 22 °C hasta los 30 °C, la temperatura óptima se sitúa en los 26 °C (Madeira et al., 2016). Un hallazgo crítico de Versteeg et al. (2025) revela que, ante olas de calor marinas o estrés térmico extremo, el A. percula posee la capacidad de «encogerse» de forma reversible como mecanismo de supervivencia, una respuesta fisiológica que resalta la importancia de evitar fluctuaciones bruscas.
Estrategias de Salinidad y Eficiencia Operativa
La viabilidad de la cría en agua salobre ha abierto nuevas puertas económicas. Carneiro et al. (2024) confirmaron que los juveniles de A. ocellaris pueden desarrollarse con una supervivencia superior al 95% en salinidades de tan solo 15‰.
- Beneficio Económico: Esta estrategia permite reducir hasta en un 57% los costos en sales marinas comerciales.
- Límite de Tolerancia: Es vital no descender de las 10 ppt, ya que, según Salleh et al. (2024), este es el umbral crítico para la supervivencia de la especie.
Toxicidad y Compuestos Nitrogenados
El control del amoníaco y los nitritos es la prioridad número uno en sistemas de recirculación (RAS). Para el pez payaso granate (Premnas biaculeatus), el amoníaco no ionizado presenta una letalidad (LC50) de 0.89 mg/L a las 96 horas (Rodrigues et al., 2014). En términos generales, se recomienda mantener niveles de amoníaco inferiores a 0.57 mg/L y nitritos por debajo de 25 mg/L para evitar daños tisulares (Medeiros et al., 2019).
Ficha Técnica de Referencia
La siguiente tabla resume los valores esenciales para la gestión de un sistema de cría:
| Parámetro | Rango / Valor Recomendado |
| Tamaño del Acuario (1♀ / 4♂) | Mínimo 70 litros |
| Temperatura del Agua | Óptima: 26 °C (Rango: 22 – 30 °C) |
| Salinidad (Gravedad Específica) | 1.023 – 1.025 SG (o 15-35‰ según objetivo) |
| pH del Agua | 8.0 – 8.5 |
| Amoníaco (NH₃) | 0 mg/L |
| Nitritos (NO₂) | < 0.1 mg/L |
| Fotoperiodo | 12h Luz / 12h Oscuridad |
Compatibilidad y Dinámicas de Convivencia
El comportamiento social de los peces payaso es tan fascinante como complejo. Su sistema de comunicación, basado en estímulos acústicos (chasquidos), les permite coordinar una jerarquía interna sumamente organizada. Generalmente, estos grupos están compuestos por una hembra dominante, un macho reproductor y una cohorte de individuos juveniles de menor tamaño.
El Mecanismo de Sucesión
La estabilidad del grupo está garantizada por su plasticidad biológica. Según reporta la Great Barrier Reef Foundation, si la hembra dominante fallece, el macho de mayor rango inicia una transición biológica permanente para convertirse en la nueva hembra. Simultáneamente, el individuo más grande entre los juveniles asume el rol de macho dominante, asegurando la continuidad del ciclo reproductivo en el arrecife.
Territorialidad y Agresión
En su hábitat natural, los peces anémona son fuertemente territoriales. Defienden su anfitrión con una tenacidad sorprendente y rara vez se alejan de la protección de sus tentáculos. De acuerdo con el Aquarium of the Pacific, los patrones de agresión —orientados a expulsar intrusos de su zona de influencia— incluyen:
- Golpeo de cola (tail-slapping).
- Persecuciones constantes.
- Mordeduras dirigidas a la cabeza, el abdomen y las aletas del competidor.
Selección de Compañeros de Tanque
Para garantizar un entorno pacífico en el acuario doméstico, la selección de compañeros debe basarse en la compatibilidad de temperamento y la similitud de requisitos ambientales. Se recomienda evitar especies excesivamente agresivas o de gran tamaño que puedan competir directamente por el territorio.
Compañeros recomendados:
- Gobios y Blénidos: Especies bentónicas que suelen ocupar zonas distintas del acuario.
- Lábridos pequeños: Peces activos que comparten un temperamento compatible.
Nota de manejo: Independientemente de la especie, es imperativo introducir a los nuevos integrantes de forma gradual y monitorear sus interacciones durante los primeros días para prevenir conflictos territoriales agudos.
Patologías Comunes y Gestión Sanitaria
La prevención y el diagnóstico temprano son pilares fundamentales para mantener la salud de las poblaciones de peces payaso en cautiverio. A continuación, se detallan las afecciones virales y parasitarias de mayor incidencia reportadas recientemente.
Amiloodiniosis (Oodiniosis)
Esta enfermedad parasitaria es una de las mayores amenazas en sistemas de recirculación. Dhayanithi et al. (2022) han documentado brotes severos de amiloodiniosis específicamente en el pez payaso percula (A. percula).
- Protocolo de Tratamiento: Los investigadores recomiendan la aplicación terapéutica de sulfato de cobre a una concentración de 10 ppm para erradicar eficazmente el parásito y controlar la propagación del brote.
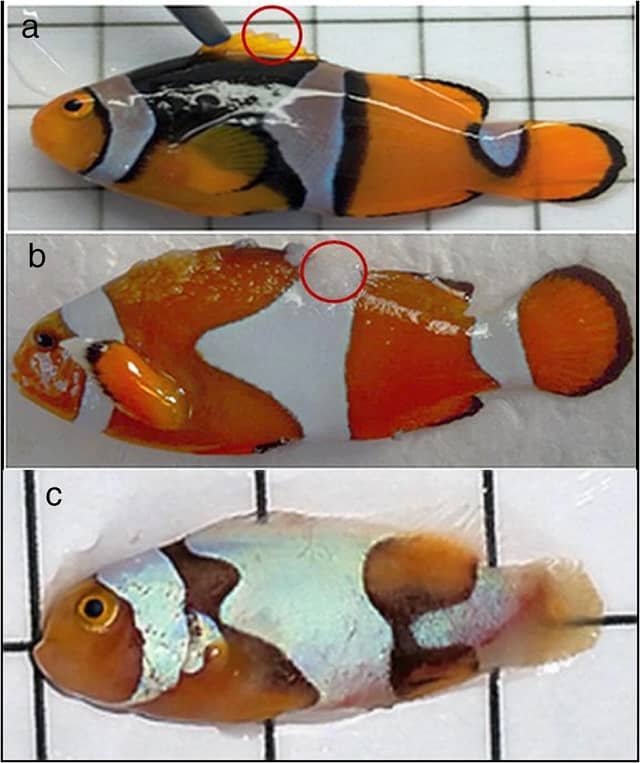
Linfocistis (LCDV)
La linfocistis es una patología de origen viral que afecta a diversas especies, habiéndose reportado casos en A. percula (Lam et al., 2020), así como en A. ocellaris y A. clarkii (Cheng et al., 2023).
- Diagnóstico: Las investigaciones moleculares han confirmado la presencia del virus de la enfermedad de la linfocistis (LCDV) en los tejidos infectados, lo que subraya la importancia de mantener protocolos de bioseguridad para evitar la transmisión viral entre tanques.
- Signos Clínicos: Según las observaciones de Lam et al. (2020), los ejemplares afectados presentan manchas blancas características y formaciones similares a verrugas en la dermis y las aletas.
Malformaciones y Anomalías del Desarrollo
El control térmico en la acuicultura es un arma de doble filo: aunque acelera el metabolismo, un exceso de temperatura puede comprometer la integridad estructural de los ejemplares. Investigaciones recientes han cuantificado este riesgo con precisión.
El Impacto de la Temperatura en la Osteología
Según los hallazgos de Rodríguez-Ibarra et al. (2024), existe una correlación directa entre el incremento térmico y la incidencia de deformidades esqueléticas. Los datos revelan un umbral crítico de seguridad:
- Incidencia Crítica: El nivel más alto de malformaciones (13.3%) se registra en larvas cultivadas a 34 °C.
- Rango de Seguridad: El porcentaje de anomalías se reduce drásticamente al 1.2% cuando el cultivo se mantiene a una temperatura estable de 28 °C.
Tipología de las Deformaciones
El estudio detalla las patologías óseas más recurrentes observadas durante el desarrollo larval bajo condiciones de estrés térmico:
- Lordosis: Es la deformidad de mayor frecuencia (11%), caracterizada por una curvatura anormal de la columna hacia adentro.
- Anomalías en Aletas: Malformaciones en las estructuras dorsales y anales alcanzaron un 9.4%.
- Cifosis: Curvatura hacia afuera de la columna, presente en el 7.6% de los casos.
- Escoliosis: Desviaciones laterales de la columna vertebral, registradas en un 6.4% de la muestra.
Estos resultados sugieren que, para garantizar una producción de alta calidad comercial y ética, los criadores deben priorizar la estabilidad térmica por encima de la velocidad de crecimiento.
Conclusión
La crianza del pez payaso es una labor profundamente gratificante que permite integrar la biodiversidad del océano en un entorno controlado. Al profundizar en sus necesidades biológicas únicas, garantizar un hábitat técnicamente adecuado y mantener una calidad de agua inmejorable, usted podrá crear un ecosistema donde estas icónicas criaturas no solo sobrevivan, sino que prosperen y se desarrollen con plenitud.
Desde la configuración estratégica del acuario y el diseño de una dieta equilibrada, hasta la selección precisa de compañeros compatibles, esta guía técnica le ha proporcionado el rigor científico y la confianza necesaria para liderar un proyecto de acuicultura o acuarismo doméstico con éxito.
Le invitamos a sumergirse en este fascinante desafío, aplicando los últimos avances en investigación para crear un refugio submarino que cautive los sentidos y garantice el bienestar de sus ejemplares.
Preguntas Frecuentes (FAQ) sobre el Pez Payaso
¿Realmente todos los peces payaso nacen machos?
Sí, los peces payaso son hermafroditas protándricos. Esto significa que todos nacen con órganos sexuales masculinos. La transición a hembra solo ocurre por una necesidad jerárquica (cuando la hembra dominante muere) y es un proceso biológico irreversible gobernado por el modelo ARCH.
¿Cuál es la temperatura ideal para que no tengan malformaciones?
Aunque pueden tolerar rangos amplios, los estudios de 2024 indican que el «punto dulce» para evitar malformaciones es de 28 °C. Si bien a 34 °C crecen más rápido, el riesgo de deformidades óseas como la lordosis aumenta significativamente hasta un 13.3%.
¿Es obligatorio usar Artemia para alimentar a las larvas?
No necesariamente. Según las investigaciones de Murray et al. (2025), es posible realizar un destete temprano a microdietas inertes a partir de los 5 días posteriores a la eclosión (DPH). Esto elimina la dependencia de la Artemia, reduciendo costos operativos sin afectar la supervivencia.
¿Cómo puedo intensificar el color de mis peces?
La clave está en la suplementación con carotenoides. Se recomienda un mínimo de 0.5% de astaxantina en la dieta. Avances recientes sugieren que el uso de extractos naturales de fruto de Gac o pimiento morrón puede incrementar la intensidad del color rojo entre un 75% y un 89%.
¿Por qué mi pez payaso es agresivo con otros peces?
La agresividad es un comportamiento natural vinculado a la defensa de su territorio y su anémona. Utilizan chasquidos para comunicarse y ataques físicos (mordeduras y persecuciones) para expulsar intrusos. Para minimizar esto, se recomienda introducir primero al macho más pequeño en el tanque.
¿Qué importancia tiene la oscuridad en la eclosión de los huevos?
La oscuridad absoluta es el detonante biológico para que los embriones secreten las enzimas de eclosión. Sin este periodo de oscuridad, la eclosión puede retrasarse o ser asincrónica, afectando la viabilidad de la puesta.
Referencias bibliográficas
Aquarium of the Pacific. Clownfish: Amphiprion ocellaris
Arossa S, Steckbauer A, Klein SG, Parry AJ, Alva Garcia JV, Alamoudi T, Pluma N, Frappi S, Duarte CM. 2025 Oxygen availability modulates clownfish larvae responses to acute thermal stress in experimental settings. Proc. R. Soc. B 292: 20252201. https://doi.org/10.1098/rspb.2025.2201
Carneiro, M. D. D., Medeiros, R. S. d., Monserrat, J. M., Rodrigues, R. V., & Sampaio, L. A. (2024). Growth and Oxidative Stress of Clownfish Amphiprion ocellaris Reared at Different Salinities. Fishes, 9(1), 30. https://doi.org/10.3390/fishes9010030
Chambel, J., Severiano, V., Baptista, T. et al. Effect of stocking density and different diets on growth of Percula Clownfish, Amphiprion percula (Lacepede, 1802). SpringerPlus 4, 183 (2015). https://doi.org/10.1186/s40064-015-0967-x
Chiodo, T., De Jode, A., Quattrini, A. M., Gibson, M. K., Froehlich, C. Y., Huang, D., Fujii, T., Yanagi, K., Reimer, J. D., Scott, A., Rodríguez, E., & Titus, B. M. Nemo knows: Clownfishes differentiate cryptic host species across fine and broad geographic scales and reveal a diverse species complex in the clownfish-hosting sea anemones. Systematic Biology. https://doi.org/10.1093/sysbio/syag033
Cheng, M.-C.; See, M.S.; Wang, P.-C.; Kuo, Y.-T.; Ho, Y.-S.; Chen, S.-C.; Tsai, M.-A. Lymphocystis Disease Virus Infection in Clownfish Amphiprion ocellaris and Amphiprion clarkii in Taiwan. Animals 2023, 13, 153. https://doi.org/10.3390/ani13010153
Dhayanithi, N.B., Sudhagar, A., Kumar, T.T.A. et al. Study on amyloodiniosis outbreak in captive-bred percula clownfish (Amphiprion percula) and improved control regimens. J Parasit Dis 46, 1103–1109 (2022). https://doi.org/10.1007/s12639-022-01530-1
Díaz-Jiménez, L., Hernández-Vergara, M.P., Pérez-Rostro, C.I. and Olvera-Novoa, M.Á. (2021), The effect of two carotenoid sources, background colour and light spectrum on the body pigmentation of the clownfish Amphiprion ocellaris. Aquaculture Research, 52: 3052-3061. https://doi.org/10.1111/are.15149
dos Santos, T.M.L., de Oliveira Sousa, E.M., Tsuzuki, M.Y. et al. Tank color influences the response of tomato clownfish (Amphiprion frenatus) to an acute stress challenge. Fish Physiol Biochem 49, 577–584 (2023). https://doi.org/10.1007/s10695-023-01203-7
Fobert Emily K., Burke da Silva Karen and Swearer Stephen E. 2019. Artificial light at night causes reproductive failure in clownfish. Biol. Lett.152019027220190272
Gaboriau, T., Marcionetti, A., Garcia-Jimenez, A., Schmid, S., Fitzgerald, L. M., Micheli, B., Titus, B., & Salamin, N. (2025). Host use drives convergent evolution in clownfish. Proceedings of the National Academy of Sciences, 122(17), e2419716122. https://doi.org/10.1073/pnas.2419716122
Great Barrier Reef Foundation. Clownfish.
Hoffmann, H., Ozório, R.Á., Lopes, R.G. et al. Natural or synthetic carotenoid: impacts of Haematococcus pluvialis-derived astaxanthin and synthetic astaxanthin on the diet of clownfish Amphiprion ocellaris. Blue Biotechnol. 2, 17 (2025). https://doi.org/10.1186/s44315-025-00041-x
Lai, Y.-R., Sun, W.-T., Pan, C.-Y., Pan, C.-H., & Ding, D.-S. (2026). Evaluation of hybridization and spawning ground between Amphiprion ocellaris and Amphiprion ocellaris var. J. Fish. Soc. Taiwan, 53(3), 34-43. https://doi.org/10.29822/JFST.202609_53(3).0003
Lam, C., Khairunissa, I., Damayanti, L. et al. Detection of a new strain of lymphocystis disease virus (LCDV) in captive-bred clownfish Amphiprion percula in South Sulawesi, Indonesia. Aquacult Int 28, 2121–2137 (2020). https://doi.org/10.1007/s10499-020-00581-6
Madeira, C., Madeira, D., Diniz, M. S., Cabral, H. N., & Vinagre, C. (2016). Thermal acclimation in clownfish: an integrated biomarker response and multi-tissue experimental approach. Ecological Indicators, 71, 280-292.
Maison, K. A., & Graham, K. S. (2016). Status review report: orange clownfish (Amphiprion percula). NOAA.
Medeiros, R.S., Lopez, B.A., Sampaio, L.A. et al. Ammonia and nitrite toxicity to false clownfish Amphiprion ocellaris . Aquacult Int 24, 985–993 (2016). https://doi.org/10.1007/s10499-015-9965-9
Medeiros, A. F. F., Cruz, V. K., Carvalho, C. V. A., Owatari, M. S., & Tsuzuki, M. Y. (2026). Simultaneous impacts of salinity and temperature on the survival, growth and metamorphosis of yellowtail clownfish (Amphiprion clarkii) during larviculture. Int Aquat Res. https://doi.org/10.22034/iar.2026.2009738.1969
Moore, B., Jolly, J., Izumiyama, M., Kawai, E., Ryu, T., & Ravasi, T. (2023). Clownfish larvae exhibit faster growth, higher metabolic rates and altered gene expression under future ocean warming. Science of The Total Environment, 873, 162296. https://doi.org/10.1016/j.scitotenv.2023.162296
Murray, C. A., Lacy, B. D., Markham, O. I., & DiMaggio, M. A. (2025). Refining Larval Culture Protocols of Clownfish (Amphiprion ocellaris) to Reduce the Use of Live Feeds. Fishes, 10(9), 461. https://doi.org/10.3390/fishes10090461
Nass, D.H., Gonçalves, E.L.T. & Tsuzuki, M.Y. Effect of live food transition time on survival, growth and metamorphosis of yellowtail clownfish, Amphiprion clarkii, larvae. Aquacult Int 24, 1255–1261 (2016). https://doi.org/10.1007/s10499-016-9982-3
Paixão, P. E. G., do Couto, M. V. S., da Costa Sousa, N., Abe, H. A., Reis, R. G. A., Dias, J. A. R., … & Fujimoto, R. Y. (2020). Autochthonous bacterium Lactobacillus plantarum as probiotic supplementation for productive performance and sanitary improvements on clownfish Amphiprion ocellaris. Aquaculture, 526, 735395.
Rahman, T. (2026). Sex change in clownfish as an ARCH-governed biological decision. Hormones and Behavior, 180, 105907. https://doi.org/10.1016/j.yhbeh.2026.105907
Rodrigues, R.V., Romano, L.A., Schwarz, M.H., Delbos, B. and Sampaio, L.A. (2014), Acute tolerance and histopathological effects of ammonia on juvenile maroon clownfish Premnas biaculeatus (Block 1790). Aquac Res, 45: 1133-1139. https://doi.org/10.1111/are.12054
Rodríguez-Ibarra, Luz Estela, Abdo de la Parra, María Isabel, Velasco-Blanco, Gabriela, Aguilar-Zárate, Gabriela, & Martínez-Brown, Juan Manuel. (2024). Effect of temperature on the incubation, growth, survival, and presence of skeletal deformities in larvae of the clownfish Amphiprion ocellaris (Pomacentridae) under rearing conditions. Latin american journal of aquatic research, 52(3), 501-507. https://dx.doi.org/10.3856/vol52-issue3-fulltext-3151
Roux, N., Salis, P., Lambert, A., Logeux, V., Soulat, O., Romans, P., … & Laudet, V. (2019). Staging and normal table of postembryonic development of the clownfish (Amphiprion ocellaris). Developmental Dynamics, 248(7), 545-568.
Roux, N, Logeux, V, Trouillard, N, et al. A star is born again: Methods for larval rearing of an emerging model organism, the False clownfish Amphiprion ocellaris. J Exp Zool (Mol Dev Evol). 2021; 336: 376– 385. https://doi.org/10.1002/jezb.23028
Salleh, K. M., Lokman, E. D., Ma’mur, D. B., Ibrahim, N. S., & Yahaya, M. Z. (2024). Effect of salinity variation on the survival rate of Amphiprion ocellaris (Common Clownfish). INTERNATIONAL JOURNAL OF RESEARCH, 8, 455-466.
Sarvi, B., & Pourmozaffar, S. (2024). A review of the reproduction and rearing of clownfish, Amphiprion clarkii, in captivity. International Journal of Aquatic Research and Environmental Studies, 4(2), 145-158.
Tartila, S. S. Q., Abdillah, A. A., & Saramoutia, A. (2023). The Clownfish (Amphiprion spp.) Larviculture Technique with Recirculating Aquaculture System (RAS) in Buleleng, Bali. Journal of Aquaculture Development and Environment, 6(1), 363-369.
Tran DV, Luong HT, Pham KT, Dang TT, Hua NT, Pham HQ. Plant-based carotenoid supplementation: Growth, feed utilization efficiency, and coloration in false clownfish (Amphiprion ocellaris). Israeli Journal of Aquaculture – Bamidgeh. 2024;76(1). doi:10.46989/001c.94193
Vargas-Abúndez, A. J., Randazzo, B., Foddai, M., Sanchini, L., Truzzi, C., Giorgini, E., … & Olivotto, I. (2019). Insect meal based diets for clownfish: Biometric, histological, spectroscopic, biochemical and molecular implications. Aquaculture, 498, 1-11.
Versteeg, M. A., MacDonald, C., Bennett-Smith, M. F., Buston, P. M., & Rueger, T. (2025). Individual clown anemonefish shrink to survive heat stress and social conflict. Science Advances. https://doi.org/adt7079
Wang, G., Liu, J., Yang, J., Ma, S., Wang, Z., He, Y., Li, X., Yin, W., Li, X., Li, J., Xu, K., Wang, C., & Xu, W. (2025). Examination of Social Behavior and Cognition in Clownfish (Amphiprion ocellaris): Relationship to Artificial Rearing of Juveniles. Fishes, 10(11), 549. https://doi.org/10.3390/fishes10110549
Yamanaka, S., Okada, Y., Furuta, T., & Kinoshita, M. (2021). Establishment of culture and microinjection methods for false clownfish embryos without parental care. Development, Growth & Differentiation, 63, 459– 466. https://doi.org/10.1111/dgd.12759
Yamanaka, S., Kawaguchi, M., Yasumasu, S., Sato, K. and Kinoshita, M. (2025), Effects of Light and Water Agitation on Hatching Processes in False Clownfish Amphiprion ocellaris. Journal of Experimental Zoology Part B: Molecular and Developmental Evolution, 344: 29-40. https://doi.org/10.1002/jez.b.23276
Editor de la revista digital AquaHoy. Biólogo Acuicultor titulado por la Universidad Nacional del Santa (UNS) y Máster en Gestión de la Ciencia y la Innovación por la Universidad Politécnica de Valencia, con diplomados en Innovación Empresarial y Gestión de la Innovación. Posee amplia experiencia en el sector acuícola y pesquero, habiendo liderado la Unidad de Innovación en Pesca del Programa Nacional de Innovación en Pesca y Acuicultura (PNIPA). Ha sido consultor senior en vigilancia tecnológica, formulador y asesor de proyectos de innovación, y docente en la UNS. Es miembro del Colegio de Biólogos del Perú y ha sido reconocido por la World Aquaculture Society (WAS) en 2016 por su aporte a la acuicultura.







