Los Sistemas de Recirculación en Acuicultura (RAS) representan un avance fundamental para la producción sostenible de salmón del Atlántico, permitiendo cultivar smolts de mayor tamaño en ambientes controlados y bioseguros. Sin embargo, la naturaleza cerrada de estos sistemas, su «talón de Aquiles», puede facilitar la acumulación y persistencia de patógenos, convirtiendo un pequeño problema en un brote a gran escala.
Tradicionalmente, la vigilancia de enfermedades se ha basado en el muestreo de tejidos, un método invasivo y a menudo letal que genera preocupaciones económicas y de bienestar animal. Ante este desafío, surge una pregunta clave: ¿es posible detectar a los enemigos invisibles del salmón simplemente analizando el agua en la que viven?
Un estudio reciente, publicado por investigadores del Faroese Food and Veterinary Authority, University of Copenhagen y de Hiddenfjord, desarrollado durante 12 semanas en una granja comercial de pre-smolts de salmón del Atlántico, evaluó el potencial del ADN y ARN ambiental (ADNe/ARNe) como una herramienta de alerta temprana. Los resultados no solo validan esta técnica no invasiva, sino que también desvelan la compleja dinámica de las infecciones múltiples en un entorno RAS.
- 1 Conclusiones clave
- 2 Un sistema RAS comercial bajo la lupa
- 3 La dinámica de las infecciones: un patógeno abre la puerta a otros
- 4 Una cascada de infecciones secundarias
- 5 Muestras de agua vs. hisopos: ¿qué tan confiable es el ADN ambiental?
- 6 Implicaciones prácticas para la salmonicultura en RAS
- 7 Entradas relacionadas:
Conclusiones clave
- El análisis de ADN/ARN ambiental (ADNe/ARNe) en el agua es una herramienta eficaz y no invasiva para la detección temprana del virus de la viruela de las branquias (SGPV) y el virus de la anemia infecciosa del salmón (ISAV-HPRO) en sistemas RAS.
- La carga viral de SGPV en el agua antes de la siembra de peces se correlacionó directamente con la gravedad y rapidez del brote, actuando como un valioso indicador predictivo.
- Se observó una dinámica de infección secuencial: un brote inicial de SGPV fue seguido por infecciones secundarias de ISAV-HPRO y del virus de la necrosis pancreática infecciosa (IPNV).
- Los patógenos pueden persistir en el ambiente del RAS entre ciclos de producción, lo que subraya la importancia crítica de la desinfección para mantener la bioseguridad del sistema.
Un sistema RAS comercial bajo la lupa
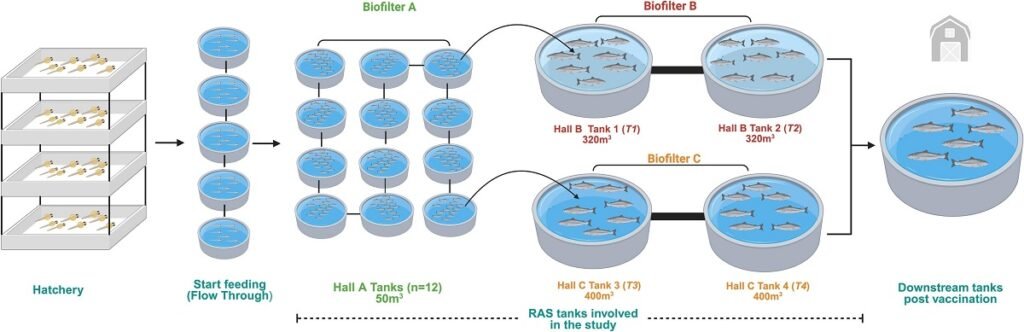
El estudio se llevó a cabo en una instalación con tres salas (A, B y C), cada una operando como un sistema RAS independiente con su propio biofiltro. Peces «vírgenes» o naïve, sin exposición previa a patógenos, fueron criados en la sala A y posteriormente transferidos a las salas B y C para su crecimiento.
Durante doce semanas, los investigadores monitorearon la presencia de cinco patógenos clave conocidos por persistir en los RAS de las Islas Feroe:
- Virus de la viruela de las branquias del salmón (SGPV)
- Virus de la anemia infecciosa del salmón no virulento (ISAV-HPRO)
- Virus de la necrosis pancreática infecciosa (IPNV)
- Piscine orthoreovirus genotipo 1 (PRV-1)
- La bacteria Flavobacterium psychrophilum
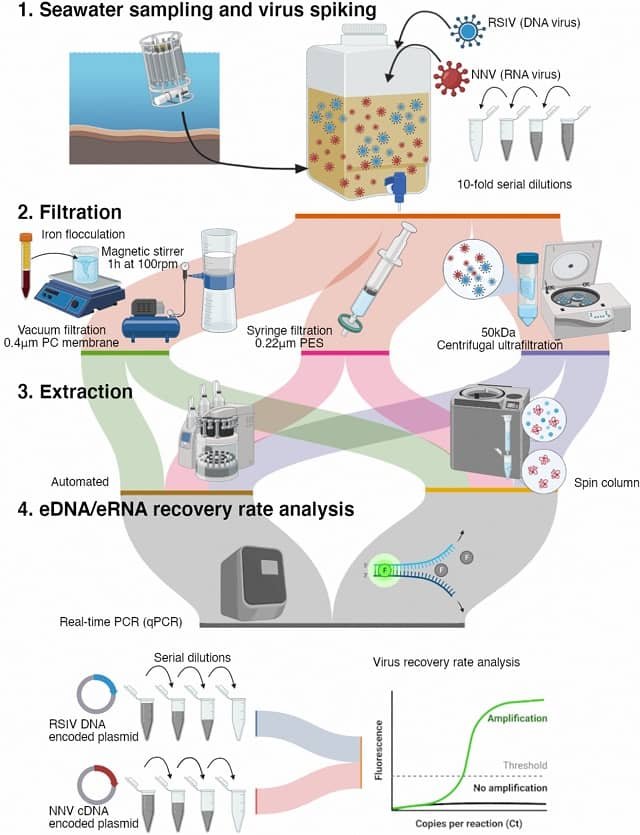
Para ello, compararon los resultados obtenidos de los hisopos de branquias y riñón de los peces con los de las muestras de agua, que fueron filtradas para capturar el material genético (ADNe/ARNe) liberado por los peces y los microorganismos en el ambiente.
La dinámica de las infecciones: un patógeno abre la puerta a otros
Los hallazgos revelaron un patrón de infección secuencial casi idéntico en las dos salas de engorde (B y C), demostrando cómo un patógeno puede debilitar a los peces y facilitar la entrada de otros.
SGPV: el detonante principal
El primer patógeno en aparecer fue el SGPV, causando una infección clínica. La diferencia clave entre las dos salas fue la carga viral inicial en el agua. Antes de introducir a los peces, las muestras de agua de la sala B ya mostraban niveles de SGPV 100 veces más altos que los de la sala C.
Esta diferencia inicial tuvo consecuencias drásticas:
Mantente siempre informado
Únete a nuestras comunidades para recibir al instante las noticias, informes y análisis más importantes del sector acuícola.
- En la sala B: La infección por SGPV se desarrolló rápidamente, alcanzando su pico a los 9 días post-introducción y provocando un fuerte aumento de la mortalidad.
- En la sala C: Con una carga viral inicial baja, la infección progresó lentamente, alcanzando su pico a los 23 días y sin causar un aumento significativo de la mortalidad.
Este resultado es crucial, ya que demuestra que la cuantificación de SGPV en el agua puede funcionar como un indicador predictivo de la gravedad de un futuro brote.
Una cascada de infecciones secundarias
Tras el pico de infección por SGPV, los peces se volvieron vulnerables a otros patógenos. En la sala B, la más afectada, se observó un aumento concurrente de ISAV-HPRO e IPNV después de 22 días. La bacteria oportunista F. psychrophilum también mostró pequeños picos de infección después del brote de SGPV en ambas salas.
Esta secuencia sugiere que la infección por SGPV podría suprimir el sistema inmune de los peces, creando una ventana de oportunidad para infecciones secundarias que complican el cuadro clínico.
Muestras de agua vs. hisopos: ¿qué tan confiable es el ADN ambiental?
El objetivo principal del estudio era validar el ADNe/ARNe como alternativa al muestreo de tejidos. Los resultados variaron según el tipo de patógeno, ofreciendo una guía clara sobre cómo utilizar esta herramienta.
Fuerte correlación para patógenos branquiales
Para los dos virus que afectan principalmente a las branquias, SGPV e ISAV-HPRO, se encontró una fuerte correlación positiva entre la carga viral detectada en los hisopos branquiales y la detectada en las muestras de agua. Esto significa que el análisis del agua refleja de manera fiable y precisa el estado de la infección en la población de peces. La razón es que las células epiteliales de las branquias infectadas se desprenden activamente al agua, liberando el material genético del virus y del propio pez, que puede ser capturado y analizado.
Detección de patógenos internos y persistencia en el sistema
Para los patógenos de infección predominantemente interna, como IPNV y PRV-1, no se encontró una correlación consistente entre los hisopos de riñón y las muestras de agua. Curiosamente, a menudo los investigadores detectaban niveles más altos y estables de estos virus en el agua que en los peces.
Esto no invalida la técnica, sino que cambia su interpretación: para patógenos internos, el análisis de agua es excelente para confirmar su presencia y persistencia en el ambiente del RAS, pero no necesariamente para diagnosticar el nivel de infección activo en los peces. Esto refuerza la idea de que los patógenos pueden establecer «cepas de la casa» (house strains) que recirculan y persisten en los componentes del sistema, como los biofiltros.
Implicaciones prácticas para la salmonicultura en RAS
Este estudio trasciende lo académico y ofrece herramientas directamente aplicables para los productores:
- Monitoreo predictivo: El análisis regular del agua para cuantificar el SGPV puede alertar a los productores sobre un riesgo elevado de brote incluso antes de que los peces muestren signos clínicos.
- Gestión proactiva: Basado en los hallazgos, se propone un enfoque de manejo por niveles. Por ejemplo, si los valores de Cq para SGPV en el agua caen por debajo de un umbral (ej. <25), se debe intensificar el monitoreo. Si continúan bajando, se pueden aplicar estrategias de mitigación como aumentar el recambio de agua, mejorar la oxigenación o detener la alimentación para reducir el estrés y frenar la progresión de la enfermedad.
- Mejora de la bioseguridad: La confirmación de que los patógenos persisten en el sistema subraya la necesidad crítica de protocolos de desinfección rigurosos entre los ciclos de producción para evitar la contaminación de nuevos lotes de peces.
- Bienestar animal: Al reemplazar el muestreo letal, el monitoreo con ADNe/ARNe reduce el estrés y la mortalidad de los peces, alineándose con las crecientes demandas de bienestar en la acuicultura.
En definitiva, este estudio demuestra que el análisis de agua no es una simple curiosidad científica, sino una poderosa herramienta de vigilancia que permite pasar de un manejo reactivo a uno predictivo y proactivo. La implementación de programas de monitoreo basados en ADNe/ARNe puede mejorar significativamente la bioseguridad, la salud de los peces y la sostenibilidad económica de la producción de salmón en sistemas RAS.
Contacto
Debes Hammershaimb Christiansen
National Reference Laboratory for Fish and Animal Diseases, Faroese Food and Veterinary Authority
Torshavn, Faroe Islands
Email: debesc@hfs.fo
Referencia (acceso abierto)
Krishna, D., Petersen, P. E., Dahl, M. M., Egholm, I., Von Gersdorff Jørgensen, L., & Christiansen, D. H. (2025). Environmental DNA/RNA for non-invasive early detection and monitoring of pathogen dynamics in Atlantic salmon (Salmo salar) recirculating aquaculture systems (RAS). Aquaculture, 743060. https://doi.org/10.1016/j.aquaculture.2025.743060
Editor de la revista digital AquaHoy. Biólogo Acuicultor titulado por la Universidad Nacional del Santa (UNS) y Máster en Gestión de la Ciencia y la Innovación por la Universidad Politécnica de Valencia, con diplomados en Innovación Empresarial y Gestión de la Innovación. Posee amplia experiencia en el sector acuícola y pesquero, habiendo liderado la Unidad de Innovación en Pesca del Programa Nacional de Innovación en Pesca y Acuicultura (PNIPA). Ha sido consultor senior en vigilancia tecnológica, formulador y asesor de proyectos de innovación, y docente en la UNS. Es miembro del Colegio de Biólogos del Perú y ha sido reconocido por la World Aquaculture Society (WAS) en 2016 por su aporte a la acuicultura.